Borfluoridsäure als Katalysator: Anwendungen und Mechanismen bei der Bildung von Borfluoridsalzen
Borfluoridsäure (HBF4) ist eine hochreaktive anorganische Säure, die in der modernen Chemie und Industrie eine wichtige Rolle spielt. Als Katalysator verwendet HBF4 erleichtert eine Vielzahl von Reaktionen, insbesondere solche, bei denen Borfluoridsalze entstehen, eine Klasse von Verbindungen, die in verschiedenen industriellen Anwendungen nützlich sind. In diesem Artikel untersuchen wir die spezifischen Anwendungen von Borfluoridsäure als Katalysator, ihre Rolle bei der Erleichterung chemischer Reaktionen und die zugrunde liegenden Mechanismen, die sie zu einem so vielseitigen und wirksamen Katalysator machen.
1. Was ist Borfluoridsäure und wie funktioniert sie als Katalysator?
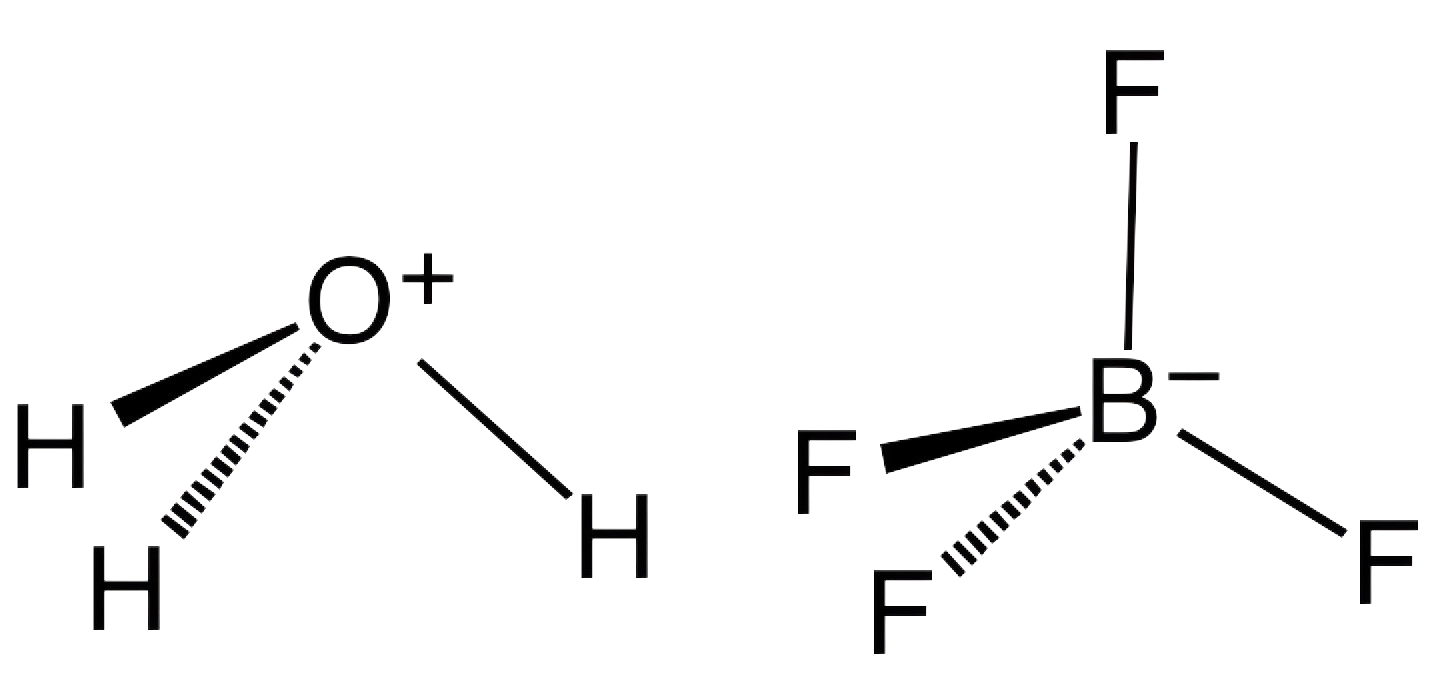
Borfluoridsäure mit der chemischen Formel HBF4ist eine Verbindung aus Wasserstoff, Bor und Fluor. Es ist eine starke Säure, die in Lösung dissoziiert und ein Proton freisetzt (H+) und das Tetrafluoroborat-Anion (BF4-). Die einzigartige Kombination von Bor und Fluor in seiner Struktur verleiht ihm ausgeprägte katalytische Eigenschaften, insbesondere bei Reaktionen, bei denen fluorbasierte Spezies oder Borchemie beteiligt sind.
Als Katalysator wirkt Borfluoridsäure, indem sie bestimmte chemische Reaktionen fördert, ohne dabei verbraucht zu werden. Sie kann Moleküle aktivieren, indem sie Protonen abgibt (als Brønsted-Säure) oder Elektronenpaare aufnimmt (als Lewis-Säure). Diese Eigenschaften machen HBF4 besonders nützlich in verschiedenen Reaktionen, einschließlich der Bildung von Borfluoridsalzen, die breite industrielle Anwendung finden.
2. Anwendungen von Borfluoridsäure als Katalysator
2.1 Bildung von Borfluoridsalzen
Eine der häufigsten Anwendungen von Borfluoridsäure ist die Synthese von Borfluoridsalzen wie Natriumtetrafluoroborat (NaBF4), Kaliumtetrafluoroborat (KBF4) und Ammoniumtetrafluoroborat (NH4BF4). Diese Salze sind für mehrere chemische Prozesse von entscheidender Bedeutung und entstehen durch Neutralisieren von Borfluoridsäure mit einer geeigneten Base. Die allgemeine Reaktion ist wie folgt:
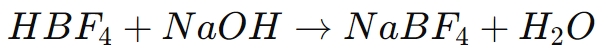
Bei diesem Prozess gibt die Fluorborsäure ein Proton an die Base ab, wodurch Wasser entsteht und das Tetrafluoroborat-Anion (BF4-), das sich dann mit dem Metallion verbindet (z. B. Na+) um ein Borfluoridsalz zu bilden.
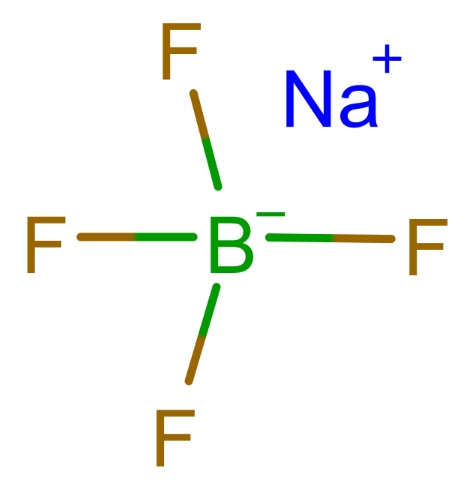
Diese Borfluoridsalze werden in verschiedenen Bereichen verwendet, unter anderem:
● Elektrochemie:Wird als Elektrolyt in Lithium-Ionen-Batterien und Galvanisierungsprozessen verwendet.
● Polymerchemie: Wirken als Initiatoren in Polymerisationsreaktionen.
● Fluorierung: Wird verwendet, um Fluoratome in organische Verbindungen einzuführen und so deren Stabilität und Reaktivität zu verbessern.
2.2 Organische Synthese und Katalyse
Borfluoridsäure spielt auch eine wichtige Rolle in der organischen Synthese, insbesondere bei der Aktivierung elektrophiler Reagenzien. Bei Verwendung als Katalysator kann HBF4 kann Reaktionen wie Friedel-Crafts-Alkylierung, Acylierung und andere elektrophile Substitutionsreaktionen beschleunigen. Der Mechanismus beinhaltet typischerweise die Lewis-Säure-Eigenschaften von HBF4, wo es sich mit elektronenreichen Spezies koordiniert, deren Reaktivität erhöht und die Bildung neuer Bindungen fördert.
Beispielsweise in derFriedel-Crafts-Alkylierung, HBF₄aktiviert Alkylhalogenide und erleichtert die Addition von Alkylgruppen an aromatische Ringe. Die allgemeine Reaktion für einen solchen Prozess ist:
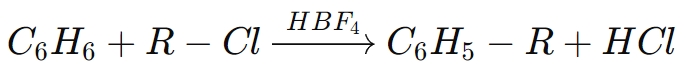
Bei dieser Reaktion fungiert Borfluoridsäure als Katalysator, der die Alkylierung von Benzol mit einem Alkylchlorid erleichtert, wodurch eine alkylierte aromatische Verbindung entsteht.
2.3 Polymerisation und Oligomerisierung
HBF4 ist auch ein wirksamer Katalysator für Polymerisationsreaktionen. Insbesondere wird es verwendet, um die Polymerisation von Styrol und anderen Monomeren zu initiieren, was zur Bildung wertvoller Polymermaterialien wie Polystyrol führt. Borfluoridsäure kann die Doppelbindung im Monomer aktivieren, was das Wachstum von Polymerketten und die Bildung des Polymers ermöglicht.
Beispielsweise bei der Polymerisation von Styrol (C8H8):
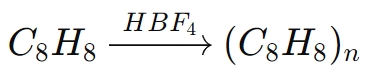
Bei dieser Reaktion wird HBF4leitet die Polymerisation durch Abgabe eines Protons an das Styrolmolekül ein, wodurch ein reaktives Carbokation entsteht, das dann die Polymerkette fortpflanzt.
Darüber hinaus kann Borfluoridsäure katalysierenOligomerisierung, der Prozess, bei dem kleine Moleküle (Oligomere) längere Ketten bilden, ohne vollständig zu polymerisieren. Dies ist wichtig bei der Herstellung von Spezialmaterialien, die in Beschichtungen und Klebstoffen verwendet werden.
2.4 Elektrochemische und Batterieanwendungen
Im Bereich der Elektrochemie wird Borfluoridsäure häufig zur Herstellung von Borfluoridsalzen verwendet, die als Elektrolyte in Lithium-Ionen-Batterien und anderen Batterietypen dienen. Der Einsatz von Borfluoridsalzen in Batterien verbessert deren Ionenleitfähigkeit und Stabilität, wodurch sie sich hervorragend für den Einsatz in Energiespeichersystemen eignen.
Beispielsweise Lithiumtetrafluoroborat (LiBF4) wird aufgrund seiner hohen Ionenleitfähigkeit und Stabilität bei hohen Spannungen häufig als Elektrolyt in Lithium-Ionen-Batterien verwendet.
Die Rolle der Borfluoridsäure in elektrochemischen Prozessen erstreckt sich auch auf die Metallgalvanisierung, bei der Borfluoridsalze als Elektrolytlösungen wirken, die die Abscheidung von Metallen wie Kupfer, Gold und Zinn erleichtern. Die Verwendung von Borfluoridsäure in diesem Zusammenhang trägt dazu bei, gleichmäßigere Beschichtungen auf Metallen zu erzeugen, was sie zu einem wesentlichen Bestandteil in Branchen wie der Elektronik und der Metallveredelung macht.
2.5 Fluorierung organischer Verbindungen
Eine weitere wichtige Anwendung von Borfluoridsäure als Katalysator sind Fluorierungsreaktionen. Die Fähigkeit, Fluoratome in organische Moleküle einzubauen, ist bei der Herstellung von Arzneimitteln, Agrochemikalien und Spezialmaterialien wertvoll. Borfluoridsäure kann Fluorquellen wie Fluorgas oder fluorhaltige Verbindungen aktivieren und ihnen ermöglichen, mit organischen Substraten zu reagieren.
Beispielsweise bei der Fluorierung einer organischen Verbindung (RX):
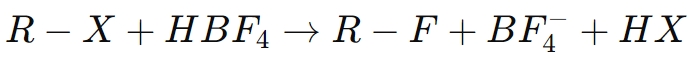
Hier erleichtert Borfluoridsäure den Ersatz eines Halogenatoms durch Fluor und verbessert so die Eigenschaften der entstehenden Verbindung, etwa ihre chemische Stabilität und Widerstandsfähigkeit gegen Abbau.
3. Mechanismus der Katalyse durch Borfluoridsäure
Die katalytische Aktivität der Borfluoridsäure erklärt sich aus ihrer Fähigkeit, sowohl alsBrønsted-Säure und einLewis-Säure:
● Brønsted-Säure: Als Protonenspender kann Fluorborsäure Substrate protonieren, wodurch ihre Elektrophilie steigt und sie in nachfolgenden Reaktionen reaktiver werden. Dies ist insbesondere bei Reaktionen wie der nukleophilen Substitution nützlich, bei der ein elektronenreiches Nukleophil ein elektrophiles Substrat angreift.
● Lewis-Säure: Borfluoridsäure wirkt als Lewis-Säure, indem sie Elektronenpaare von nukleophilen Spezies akzeptiert, wodurch Elektrophile aktiviert und verschiedene Substitutions- und Additionsreaktionen erleichtert werden. Dies ist besonders deutlich bei Reaktionen wie der Friedel-Crafts-Alkylierung, bei der HBF₄ mit Alkylhalogeniden koordiniert und diese reaktiver mit aromatischen Verbindungen macht.
Durch diese Mechanismen kann Borfluoridsäure die Aktivierungsenergie von Reaktionen senken, die Reaktionsgeschwindigkeit erhöhen und die Ausbeute der gewünschten Produkte verbessern.
4. Vorteile und Herausforderungen der Verwendung von Borfluoridsäure
4.1 Vorteile
● Effizienz:Borfluoridsäure beschleunigt Reaktionen durch Senkung der Aktivierungsenergie, was zu schnelleren Reaktionszeiten und höheren Ausbeuten führt.
● Selektivität: Seine stark sauren Eigenschaften stellen sicher, dass nur bestimmte Substrate aktiviert werden, und sorgen für eine hohe Selektivität bei komplexen Reaktionen.
● Vielseitigkeit: Es kann in zahlreichen Reaktionen eingesetzt werden, darunter organische Synthese, Polymerisation und elektrochemische Prozesse.
4.2 Herausforderungen
● Korrosivität: Aufgrund ihrer stark säurehaltigen Natur ist Borfluoridsäure hochgradig ätzend und erfordert spezielle Handhabung und Ausrüstung.
● Umweltauswirkungen: Da es sich bei Borfluoridsäure und ihren Derivaten um fluorhaltige Verbindungen handelt, müssen sie sorgfältig entsorgt werden, um eine Kontamination der Umwelt zu vermeiden.
● Kosten: Die Herstellung und Reinigung von Borfluoridsäure kann kostspielig sein, was ihre Verwendung in großindustriellen Prozessen einschränkt.
Borfluoridsäure ist ein unglaublich vielseitiger Katalysator, der eine entscheidende Rolle bei der Synthese von Borfluoridsalzen, der organischen Synthese, der Polymerisation und elektrochemischen Anwendungen spielt. Ihre Fähigkeit, sowohl als Brønsted- als auch als Lewis-Säure zu wirken, macht sie zu einem unverzichtbaren Werkzeug in vielen chemischen Prozessen. Aufgrund ihrer korrosiven Natur und ihrer Umweltauswirkungen ist bei ihrer Verwendung jedoch eine sorgfältige Handhabung erforderlich. Mit fortschreitender Forschung und technologischen Fortschritten wird Borfluoridsäure wahrscheinlich noch mehr Anwendungen in verschiedenen Branchen finden und Innovation und Effizienz in einer Vielzahl von Sektoren vorantreiben.




